A tabela periódica pode crescer para sempre? Ou há um limite para o tamanho dos átomos?
Em 2019, a tabela periódica fez 150 anos. Será que ela tem um fim? Ou núcleo de átomo é coração de mãe: sempre cabe mais um?
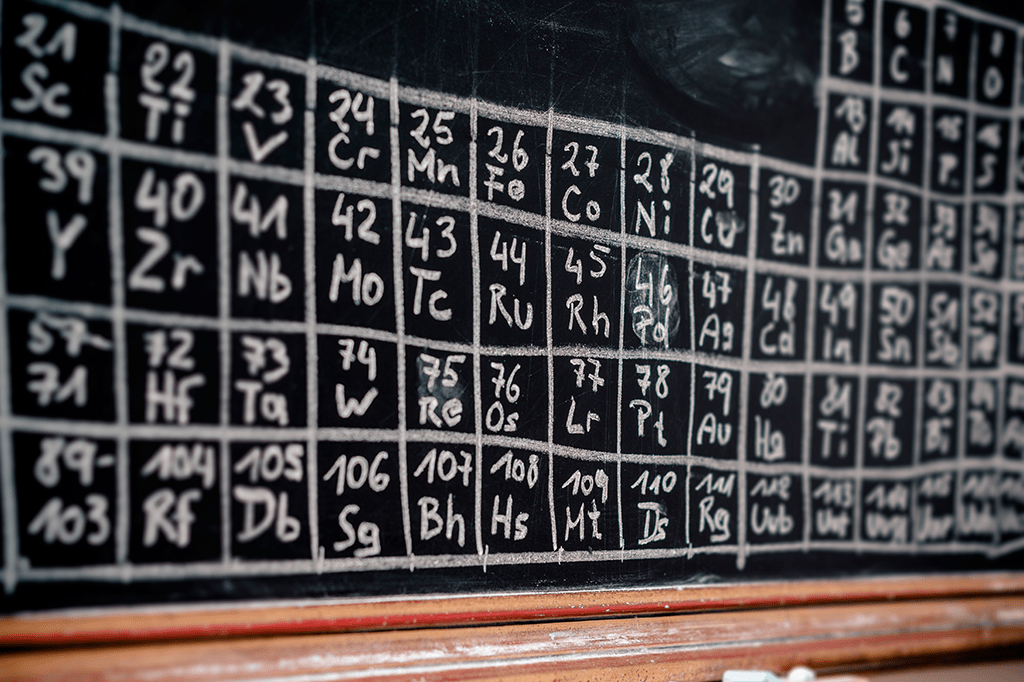
No início, era o hidrogênio, uma pitada de hélio e só. O Universo, alguns milhões de anos após o Big Bang, era um lugar notavelmente monótono para um químico. A tabela periódica dessa época tinha basicamente dois quadradinhos. Os dois átomos mais simples: um com um único próton no núcleo (o hidrogênio), outro com dois (o hélio). De lá até aqui, porém, as coisas ficaram mais interessantes. Afinal, na natureza, é só dar tempo ao tempo que tudo vai do mais simples ao mais complexo (você mesmo, não se esqueça, era uma célula até outro dia – um óvulo fecundado, no caso).
Nuvens de hidrogênio massivas, incapazes de suportar a própria gravidade, começaram a desabar sobre si próprias. Quando a pressão no interior desses acúmulos de gás atingia um ponto ridículo, ela engatilhava um processo de fusão nuclear: quatro átomos de hidrogênio passavam a se unir para formar um de hélio, liberando uma quantidade mastodôntica de radiação no processo. A essas bolas de hidrogênio gigantes, que brilham por milhões (ou até bilhões) de anos, damos o nome de “estrelas”.
É graças a elas que o Universo começa a se tornar um lugar mais fascinante para Walter White. É que estrelas são usinas de produção de elementos químicos. As forjas da tabela periódica. As maiores – várias vezes maiores que o Sol, que fique claro –, quando chegam ao final da vida, não se limitam a fundir hidrogênio para formar hélio. Elas fundem hélio para formar carbono, com seis prótons. Carbono para formar oxigênio. Oxigênio para formar silício. Silício para formar ferro (26 prótons). É no coração dessas gigantes que nasceram os átomos que compõem seu corpo – como Carl Sagan não cansou de lembrar.
Algumas estrelas, as mais gordinhas, terminam a vida com uma explosão cataclísmica: uma supernova, o título-trocadilho fúnebre deste blog. As supernovas são eventos absurdamente enérgicos, de brilho que supera as próprias galáxias que as contém. Produzem elementos novos por nucleossíntese – o jeito bonito de dizer que elas apertam dois átomos juntos até eles se unirem para formar um maior. É aí, no meio dessa violência inconcebível na escala humana, que nascem magnésio, cálcio, potássio…
Só isso, porém, não basta. E o ouro, com seus 79 prótons no núcleo? Ou o urânio, com escandalosos 92? Aí é preciso aumentar um pouco a força da pancada. Depois que uma estrela de alta massa morre no boom descrito acima, podem sobrar duas coisas à título de cadáver. Uma é um buraco negro. Outra é uma estrela de nêutrons. Uma estrela de nêutrons é um corpo tão denso, mas tão denso, que um pedacinho dela do tamanho de uma caixa de fósforo pesaria bilhões de toneladas.
Volta e meia duas estrelas de nêutrons se chocam. Pois é. Alguém anotou a placa? Nós sabemos disso porque a energia liberada gera perturbações no próprio tecido do espaço-tempo: as tais ondas gravitacionais. Numa colisão dessas, é inevitável, elementos muito pesados são formados. Gosta dos seus brincos? Ainda bem. Fabricá-los foi difícil. Metais preciosos não são raros à toa.
A massa dos elementos na tabela periódica continua crescendo: o urânio o mais gordinho dos átomos que ocorrem na natureza, tem 92 prótons em seu núcleo. Se você quiser algo mais pesado do que isso, nenhum fenômeno astronômico poderá te ajudar: serão necessários um laboratório e uma pós-graduação em física nuclear.
Laboratório e gente com pós-graduação é o que não falta nesse mundo, então, como você imaginou, elementos gordíssimos já foram produzidos artificialmente. O mais famoso deles – ainda que bastante obscuro – talvez seja o amerício (Am), sintetizado pela primeira vez na década de 1940. Daí para frente, é festa. O maior átomo já gerado em uma situação experimental atende por Oganesson (Og) e tem 118 prótons no núcleo. No papel, ele é um gás nobre – ou seja: apesar de ser uma bizarra criação humana, haveria alguma chance de que tivesse propriedades similares ao do hélio.
O problema é que um átomo de Oganesson não pode existir por tempo suficiente para medirmos suas propriedades com precisão. Ele é tão instável que dura apenas 0,89 milissegundo. O que acontece se alguém tentar forçar um número de prótons ainda maior em um núcleo? Quanto tempo eles aguentam juntos antes do átomo gigante se desfazer? Ele chega a se formar? Para dar início às comemorações de aniversário da tabela periódica, que completa 150 anos em 2019, o físico polonês Witold Nazarewicz discutiu essas e outras boas perguntas em um artigo publicado no começo de junho na Nature.
Segundo previsões teóricas mencionadas por Nazarewicz, o Oganesson, caso durasse, dificilmente seria um gás (muito menos nobre). O mundo seguro da tabela periódica, nessa escala, começa a se desfazer. Um átomo muito maior do que o Oganesson desapareceria tão rápido que não teria tempo de acumular elétrons suficientes em volta de si próprio para ser considerado… bem, um átomo. Afinal, nem só de prótons vivem os átomos: eles também precisam de elétrons em torno de si para terem propriedades químicas definidas. E o acúmulo de elétrons demora, de acordo com uma convenção estabelecida na década de 1990, 10–14 segundos. Nunca criamos um núcleo massivo o suficiente para testar esse limite temporal.
Eu não vou tomar partido: a discussão em torno da definição de elementos pesados já rendeu até um capítulo de livro. A moral da história é: a tabela periódica fica muito, muito legal quando começamos a pôr mais e mais prótons na conta. E só tem um jeito de descobrir o limite: chegando nele.


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 9 filmes imperdíveis para assistir no Prime Video
9 filmes imperdíveis para assistir no Prime Video Por que existe a letra “h” se ela não tem som?
Por que existe a letra “h” se ela não tem som? Filtro de luz azul para telas não tem eficácia comprovada
Filtro de luz azul para telas não tem eficácia comprovada Qual é o modelo de celular mais vendido da história?
Qual é o modelo de celular mais vendido da história? A cidade subterrânea de 2 mil anos e 8 andares em Derinkuyu, na Turquia
A cidade subterrânea de 2 mil anos e 8 andares em Derinkuyu, na Turquia