Como é o processo de desenvolvimento de um novo medicamento?
Com muita pesquisa e muito dinheiro

ILUSTRA Bruno Ferreira
EDIÇÃO Felipe van Deursen e Luiza Wolf
Todo o processo dura, em média, 14 anos e passa por quatro etapas bem rigorosas, que vão desde a pesquisa básica até os famosos testes clínicos. Vários agentes são envolvidos: governo, universidades, laboratórios, agências regulatórias e, claro, cobaias (animais e humanas). O custo de tudo isso pode chegar a espantosos US$ 2 bilhões. Com o perdão do trocadilho, desenvolver um novo medicamento é dose!
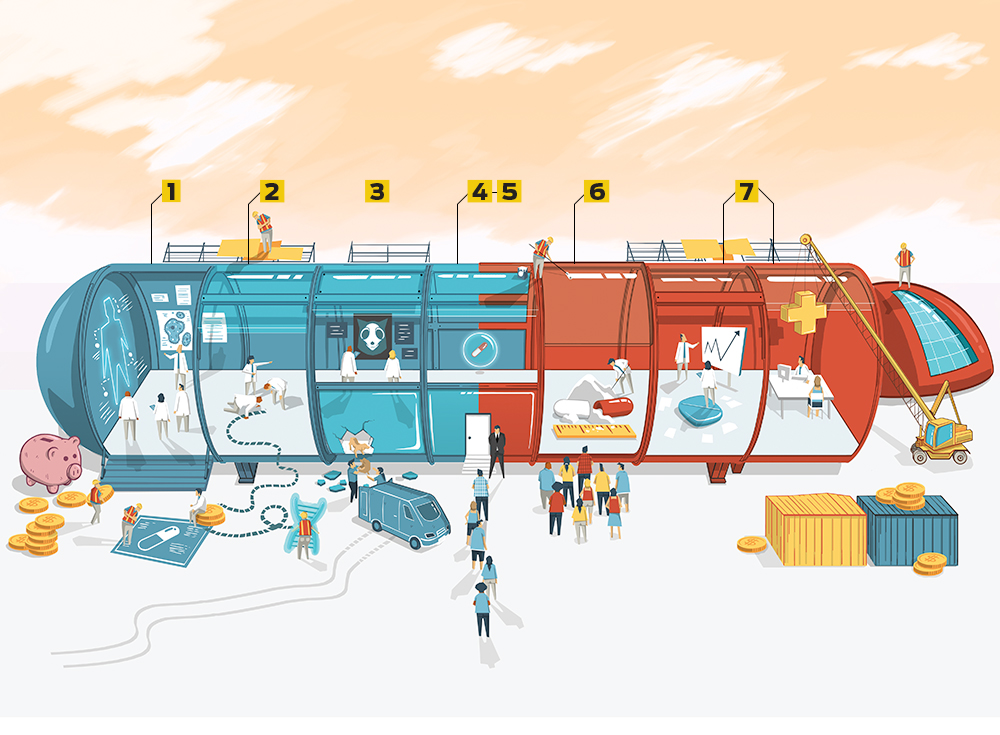
1. TIRO AO ALVO
O processo começa com a identificação de alvos, que são proteínas associadas ao desenvolvimento da doença. Elas podem vir de microrganismos causadores ou das proteínas do próprio corpo humano – nesse caso, elas podem dar sobrevida a esses microrganismos ou estar com a atividade desregulada. Essa etapa costuma ser feita em universidades, com apoio do governo e fundações. Pode durar até cinco anos e custar até US$ 25 milhões
2. ANULAÇÃO
Após descobrir a proteína responsável pela doença, deve-se rastrear compostos químicos que a combatam, a “consertem” ou inibam sua atividade. Para isso, os pesquisadores usam análises virtuais de estruturas de moléculas e experimentos com compostos que indicam a atividade das proteínas. A partir daí, fazem mais testes para escolher o que usar e como usar. Cinco de cada 5 mil compostos testados chegam à fase de ensaio clínico e somente um é aprovado
3. 1, 2, 3… TESTANDO
Hora de ver como a fórmula age em um organismo vivo. Na terceira fase, entram os polêmicos testes em modelos animais. Essa etapa é importante, porque consegue oferecer aos pesquisadores uma boa ideia da segurança, eficácia e possíveis efeitos colaterais de um novo medicamento, antes de chegar aos caríssimos ensaios clínicos em humanos
4. COBAIAS
A etapa dos ensaios clínicos é, geralmente, conduzida pela indústria farmacêutica, sob supervisão das agências regulatórias. Esses testes em humanos costumam ser divididos em três subfases. O tempo do estudo, o tamanho do grupo e o perfil dos participantes variam conforme os objetivos da empresa. Os processos mais rápidos levam até sete anos
5. MAS É SEGURO?
Basicamente, o que se faz no começo dos experimentos com cobaias é testar a droga em algumas centenas de pessoas saudáveis ou em indivíduos nos quais diversos tratamentos disponíveis falharam. Primeiro, avalia-se como o corpo reage em contato com a substância (absorção, distribuição, metabolização e eliminação); depois, qual seria a dose exata para curar o problema. Em geral, quem administra a droga e quem recebe não sabem que composto está sendo testado
6. BASE ESTATÍSTICA
Se o medicamento for bem avaliado, os testes avançam para grupos maiores (milhares de pacientes) e mais diversificados (idades e etnias diferentes). Assim, os efeitos colaterais ficam mais evidentes e mudanças na fórmula podem ser feitas. O Viagra foi inicialmente concebido para uma doença cardíaca. Mas, na fase de ensaios clínicos, os pesquisadores perceberam que um efeito colateral era, justamente, a ereção
7. ETAPA EXTRA
Os resultados devem ser aprovados pelas agências regulatórias, e os pesquisadores publicam artigos para divulgar as descobertas. Mesmo se for liberado, o remédio pode causar problemas. Em 2001, a Bayer retirou do mercado o Cerivastatin, depois que seu uso foi associado à morte de 31 pessoas nos EUA. Por isso, é comum haver uma quarta fase, a farmacovigilância, em que se acompanha de perto a experiência dos consumidores com o medicamento
CONSULTORIA Déborah Schechtman, professora associada do Departamento de Bioquímica da USP
FONTES EMS Laboratórios, Instituto Nacional de Doenças Alérgicas e Infecciosas (EUA) e Novartis



 As palavras mais bonitas do português, segundo o criador do dicionário Aurélio
As palavras mais bonitas do português, segundo o criador do dicionário Aurélio Pesquisa traz esperança para a volta dos axolotes à natureza
Pesquisa traz esperança para a volta dos axolotes à natureza Não somos máquinas de sobrevivência
Não somos máquinas de sobrevivência Por que suplementos multivitamínicos são um desperdício de dinheiro?
Por que suplementos multivitamínicos são um desperdício de dinheiro? Quais são os efeitos do café no cérebro enquanto um indivíduo dorme?
Quais são os efeitos do café no cérebro enquanto um indivíduo dorme?







