Reino Unido aprova vacina da Pfizer. Mas ela não deve chegar ao Brasil tão cedo
Segundo o Ministério da Saúde, preferência é por vacinas de dose única – e que, principalmente, não precisam ser armazenadas a temperaturas tão baixas. Entenda.
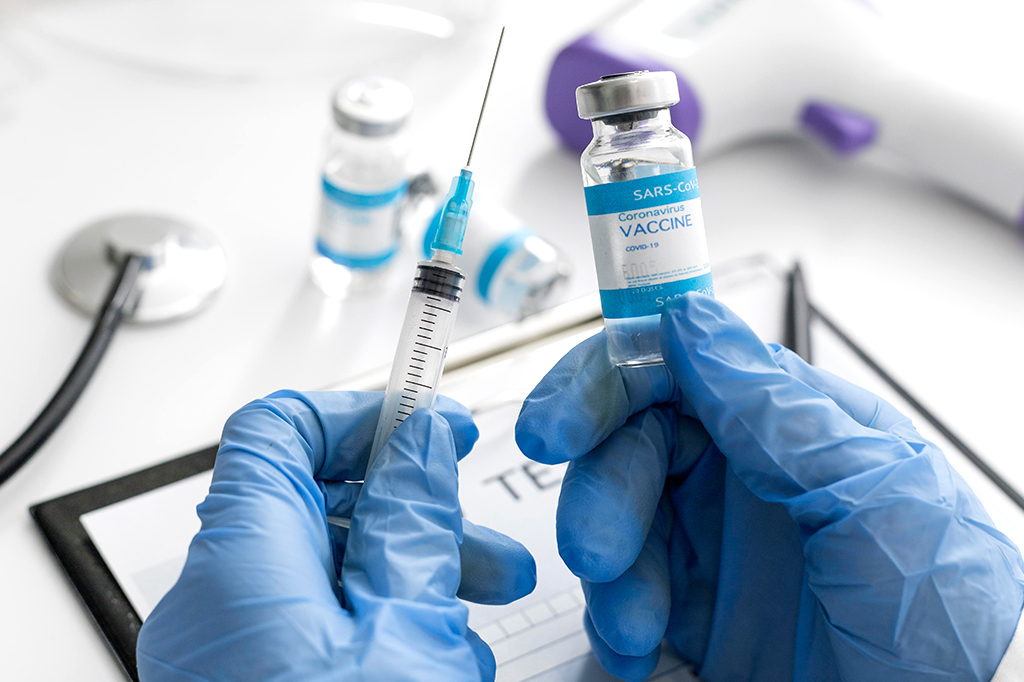
O Reino Unido se tornou o primeiro país do ocidente a liberar o uso de uma vacina contra a Covid-19. A versão aprovada no país foi a criada pela farmacêutica americana Pfizer em parceria com a alemã BioNTech. Ela apresenta eficácia de 95% contra o novo coronavírus, segundo dados clínicos divulgados há duas semanas. A decisão do Departamento de Saúde, órgão do governo britânico, foi publicada nesta quarta-feira (2).
O Reino Unido encomendou 40 milhões de doses da vacina, quantidade suficiente para vacinar 20 milhões de pessoas. De acordo com a Pfizer, a primeira parte dessa demanda, de 880 mil unidades, deve chegar ao país na próxima semana. Idosos acima dos 80 anos que vivem em casas de repouso, cuidadores e profissionais de saúde que atuam na linha de frente do combate à Covid-19 devem ter prioridade de vacinação.
Como destaca a BBC, é provável, porém, que pacientes internados em hospitais – locais com refrigeradores potentes o suficiente para armazenar a vacina – acabem passando à frente nessa fila. Diferentemente de outras candidatas a vacina, a versão da Pfizer precisa ser estocada e transportada a -70ºC. Você pode entender melhor como ela funciona – e por que só funciona se guardada sob temperaturas tão baixas – neste texto da SUPER.
Países como Rússia e China já haviam aprovado o teste de protótipos de vacinas na população sem esperar por resultados da fase 3 – etapa do desenvolvimento em que cientistas testam a eficácia de um imunizante em um grupo grande de voluntários. A liberação da vacina da Pfizer no Reino Unido, porém, representa um marco na história da epidemiologia mundial. Nunca antes uma vacina passou por todas as etapas exigidas pela ciência em tão pouco tempo. Entre a idealização, o desenvolvimento e a testagem da vacina da Moderna, foram cerca de 10 meses. Até então, a vacina de criação mais rápida havia sido a da caxumba, feita ao longo de 4 anos.
O contexto de pandemia já havia obrigado governos de países a agir rapidamente para garantir produtos como máscaras, respiradores e medicamentos com potencial de tratamento para a Covid-19. Tudo isso, por vezes, atropelando etapas burocráticas – ou até mesmo passando na frente de outros países. No caso da vacina não foi diferente. O número crescente de casos de Covid-19 no mundo serviu para agilizar, também, os trâmites legais envolvidos na liberação para o uso.
Para ser aprovada no Reino Unido, a Pfizer precisou conseguir uma autorização de emergência junto Departamento de Saúde e Cuidado Social do país. Trata-se de um processo que costuma durar meses, mas que foi cumprido no intervalo de duas semanas.
Essa autorização também está em curso na FDA, agência regulatória dos Estados Unidos – país mais afetado pela Covid-19 no mundo, com 13,8 milhões. É provável que o país seja o segundo autorizado a contar com a vacina da Pfizer – o que deve acontecer nas próximas semanas. Na terça-feira (1) a empresa americana deu entrada no processo de autorização da vacina na Europa. Depois do Reino Unido e dos EUA, países europeus devem ser os próximos a recebê-la.
E o Brasil?
Não existe uma previsão para que o Brasil passe a contar com a versão de vacina desenvolvida pela Pfizer/BioNTech. E, com base em declarações recentes do governo, é possível deduzir que o imunizante não é um dos principais alvos das campanhas de vacinação.
No dia 11 de novembro, Carlos Murillo, presidente da Pfizer no Brasil, chegou a declarar que a chegada da vacina poderia acontecer até março de 2021. Na ocasião, Murillo disse que o preço da vacina deveria ser reduzido no Brasil. As doses serão vendidas pela empresa em três faixas de preço diferentes. Países mais ricos pagarão mais caro, e os que atravessam um cenário de recessão econômica – caso brasileiro – desembolsarão menos para vacinar sua população.
Mas uma atualização colocou em xeque essa estimativa inicial. Na última terça-feira (1), o Ministério da Saúde declarou que o Plano Nacional de Imunização dará preferência para vacinas termoestáveis, que possam ser armazenadas entre 2°C e 8°C. Segundo o secretário de Vigilância em Saúde do ministério, Arnaldo Medeiros, essa temperatura de conservação é garantida nas 34 mil salas de vacinação espalhadas pelo país. Em entrevista coletiva, Medeiros afirmou também que, idealmente, a aplicação precisaria “ser feita de dose única, embora muitas vezes isso talvez não seja possível”.
Não foram citados nominalmente laboratórios ou a preferência por algum modelo de vacina. A declaração sugere, no entanto, que a vacina da Pfizer – que precisa de refrigeradores potentes para durar vários dias e requer duas doses – estaria, a princípio, fora da jogada. Ainda segundo Medeiros, o plano de imunização no Brasil só será aprovado após algum imunizante ser oficialmente registrado por aqui.
Em entrevista a CNN Brasil nesta quarta-feira (2), o diretor de vacinas da Pfizer, Alejandro Lizarraga, disse que a empresa já recebeu de pedidos países da América Latina – como Chile, Peru, Equador, México e Costa Rica – que querem ter acesso antecipado ao imunizante. “Assim que for aprovada por entidades regulatórias [dos países], vão começar a receber doses”. Segundo o porta-voz, o Brasil tem poucos dias para decidir se irá comprar a vacina se quiser receber a primeira remessa no primeiro trimestre de 2021.
Até agora, o Brasil tem acordos em andamento para a compra de 256 milhões de doses de vacinas contra a Covid-19. As duas versões que integram as negociações são a chinesa Coronavac, desenvolvida em parceria com o Instituto Butantã, e a da Universidade de Oxford – que, por aqui, vem sendo testada junto à Fiocruz. Segundo a Anvisa, pelo menos 14 milhões de doses da segunda concorrente devem ser adquiridas até fevereiro de 2021. No caso da Coronavac, as negociações vêm sendo mediadas pelo governo de São Paulo. Segundo estimativas, o estado deve receber 6 milhões de doses e produzir outras 40 milhões ainda em dezembro.


 Fallout: o que você precisa saber antes de assistir à série do Prime Video
Fallout: o que você precisa saber antes de assistir à série do Prime Video AmazonFACE: a “máquina do tempo” que levará a Amazônia para 2060
AmazonFACE: a “máquina do tempo” que levará a Amazônia para 2060 Xógum não vai ter uma segunda temporada. E não: a série não foi cancelada.
Xógum não vai ter uma segunda temporada. E não: a série não foi cancelada. Megacidade no deserto da Arábia Saudita será bem mais modesta que o previsto
Megacidade no deserto da Arábia Saudita será bem mais modesta que o previsto Marlon Brando foi o primeiro ator a ganhar um salário milionário
Marlon Brando foi o primeiro ator a ganhar um salário milionário