Anvisa altera regra de aprovação de vacinas; mudança abre espaço para Sputnik V, Moderna e Covaxin
A agência agora aceitará os resultados de estudos fase 3 realizados fora do Brasil - o que facilitará a aprovação emergencial no país de várias vacinas contra o Sars-CoV-2 .
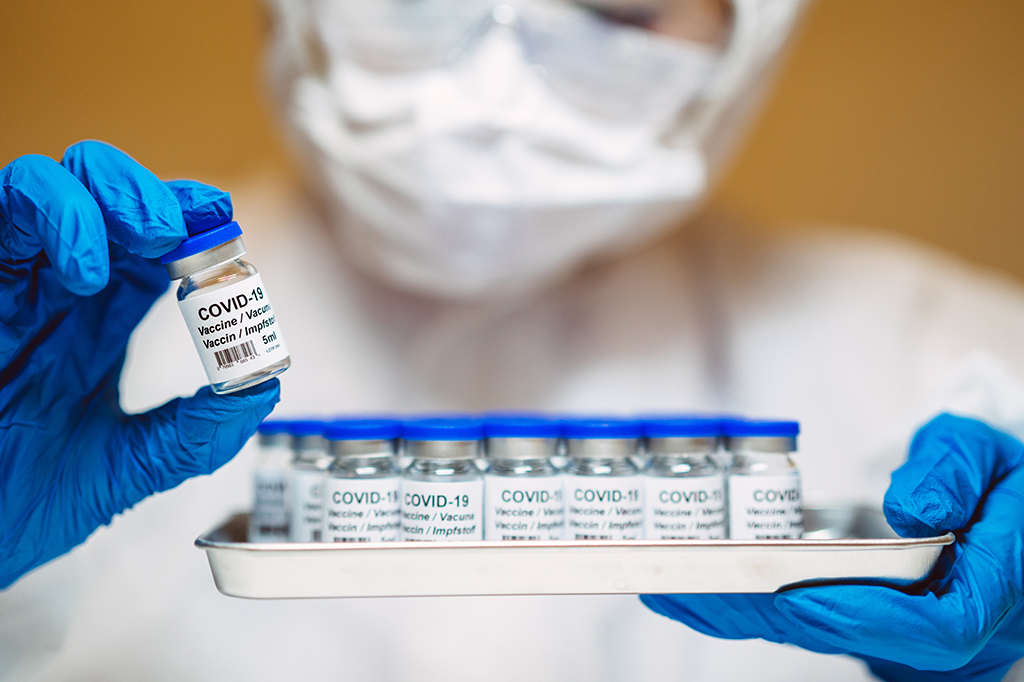
A Agência Nacional de Vigilância Sanitária (Anvisa) mudou as exigências para conceder aprovação de uso emergencial para vacinas durante a pandemia. Agora, não será pré-requisito que os testes de fase 3 do imunizante ocorram necessariamente no Brasil – estudos feitos em outros países passarão a valer também, o que facilitará a possível aprovação de vacinas como a Sputnik V. A informação foi divulgada inicialmente pela CNN Brasil e anunciada oficialmente pela agência em coletiva de imprensa no fim dessa quarta-feira (03).
A fase 3 de testes de um imunizante é a última e mais importante etapa para verificar a sua eficácia e segurança; ela envolve milhares de voluntários que são separados em dois grupos, aqueles que vão receber a vacina e os que receberão um placebo. A decisão da Anvisa não significa que essa etapa será ignorada. A novidade é que, anteriormente, exigia-se que esses estudos tivessem pelo menos começado no Brasil (total ou parcialmente), incluindo voluntários brasileiros.
Agora, estudos de fase 3 feitos exclusivamente no exterior também passam a valer, desde que atenda requisitos exigidos pela Anvisa (como seguir critérios científicos internacionais e nacionais e garantir a transparência total dos dados). A redação das novas diretrizes deixa claro que, preferencialmente, as vacinas devem ter estudos no Brasil, mas não necessariamente.
A decisão vem após uma ampla discussão sobre a necessidade da regra anterior, principalmente em meio à urgência imposta pela pandemia. A protagonista desse debate foi a Sputnik V, vacina desenvolvida pelo Instituto Gamaleya de Pesquisa, na Rússia, que anunciou ontem na revista The Lancet que seu imunizante tem 91,6% de eficácia. Por aqui, o laboratório privado União Química já firmou acordos com o instituto russo para importar doses e também produzir a vacina em solo nacional – mas enfrentava um grande obstáculo: apesar dos bons resultados, os testes não incluíram hospitais e voluntários brasileiros. A mudança de entendimento da Anvisa pode facilitar uma eventual aprovação da vacina no Brasil.
Especialistas já vinham criticando a regra há algum tempo devido à limitação que ela geraria entre as opções para a vacinação da população. Entre os imunizantes em etapas mais avançadas de testes e aprovação pelo mundo, só quatro tiveram testes feitos no Brasil: a Coronavac, da empresa chinesa Sinovac; a vacina da parceria entre a Universidade de Oxford e a britânica AstraZeneca; o imunizante da Pfizer/BioNTech; e o produzido pela Johnson & Johnson. Dessas, as duas primeiras já conseguiram aprovação para uso emergencial no país.
Com a mudança da exigência, outras candidatas entram na jogada além da Sputnik V. A Covaxin, produzida pela empresa indiana Bharat Biotech, é uma delas, além dos imunizantes produzidos pelas empresas americanas Moderna e Novavax, que também já apresentaram estudos de fase 3 em testes no exterior. Todas elas, porém, ainda precisariam passar pelo processo de aprovação normal da Anvisa, apresentando todos os documentos que comprovem sua eficácia e segurança.


 “Cem Anos de Solidão”: entenda a árvore genealógica da família Buendía
“Cem Anos de Solidão”: entenda a árvore genealógica da família Buendía Conheça a única raça brasileira de gato – confundida com “vira-lata”
Conheça a única raça brasileira de gato – confundida com “vira-lata” Estes são os 100 nomes de bebês mais populares de 2017
Estes são os 100 nomes de bebês mais populares de 2017 Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência
Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência 742 novas espécies foram identificadas em dez anos na Bacia do Congo; veja fotos
742 novas espécies foram identificadas em dez anos na Bacia do Congo; veja fotos







![[BF2024-PRORROGAMOS] - Paywall - DESKTOP - 728x90](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-DESKTOP-728x90-1.gif)
![[BF2024-PRORROGAMOS] - Paywall - MOBILE - 328x79](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-MOBILE-328x79-1.gif)