Mutação torna o coronavírus capaz de infectar mais uma espécie
Estudo revela que as variantes B.1.351 e P.1, descobertas na África do Sul e no Brasil, podem infectar ratos - que eram imunes à cepa original, de Wuhan; habilidade surgiu após alteração na proteína spike

Estudo revela que as variantes B.1.351 e P.1, descobertas na África do Sul e no Brasil, podem infectar ratos – que eram imunes à cepa original, de Wuhan; habilidade surgiu após alteração na proteína spike
A esta altura, com a pandemia entrando no segundo ano, você já deve ter ouvido falar dos receptores ACE2. Eles são formados pela “enzima conversora da angiotensina 2”, e estão presentes na membrana das células humanas (principalmente no pulmão, no coração, nos rins e nos vasos sanguíneos). Os receptores ACE2 modulam a atividade da angiotensina 2, uma proteína relacionada ao controle da pressão sanguínea e de processos inflamatórios no corpo – e, crucialmente, também servem como porta de entrada para o novo coronavírus, que se encaixa a eles para invadir as células.
O vírus precisa da ACE2 humana, ou de alguma enzima bem parecida com ela, para infectar as células. Por isso, os ratos usados para estudar o vírus em laboratório têm de ser “humanizados”, ou seja, alterados geneticamente para que produzam a ACE2 humana. Mas as mutações do Sars-CoV-2, além de deixar o vírus mais contagioso, letal e capaz de reinfectar quem já pegou cepas anteriores, deram a ele outra habilidade: a capacidade de infectar mais uma espécie.
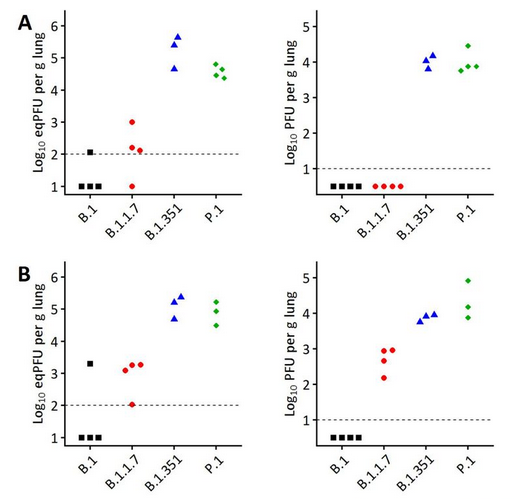
As variantes B.1.351, descoberta na África do Sul, e P.1, do Brasil, podem infectar ratos comuns, que não têm os receptores ACE2 humanos – e por isso eram imunes à cepa original do vírus, surgida em Wuhan. Foi o que constatou um estudo publicado por cientistas do Instituto Pasteur, na França.
Os pesquisadores provaram isso infectando células de rato e depois inoculando os próprios animais, que foram separados em grupos e expostos a diferentes cepas do vírus por meio de aerosol nasal. Três dias depois, os cientistas mediram a carga viral nos pulmões dos animais. A variante original não conseguiu infectar os ratos, mas as cepas B.1.351 e P.1 estavam presentes em altos níveis após 72 horas. As cobaias também foram inoculadas com a variante B.1.1.7, típica da Inglaterra. Ela conseguiu produzir infecção, mas menos potente (só ocorreu em parte dos ratos, e com carga viral mais baixa).
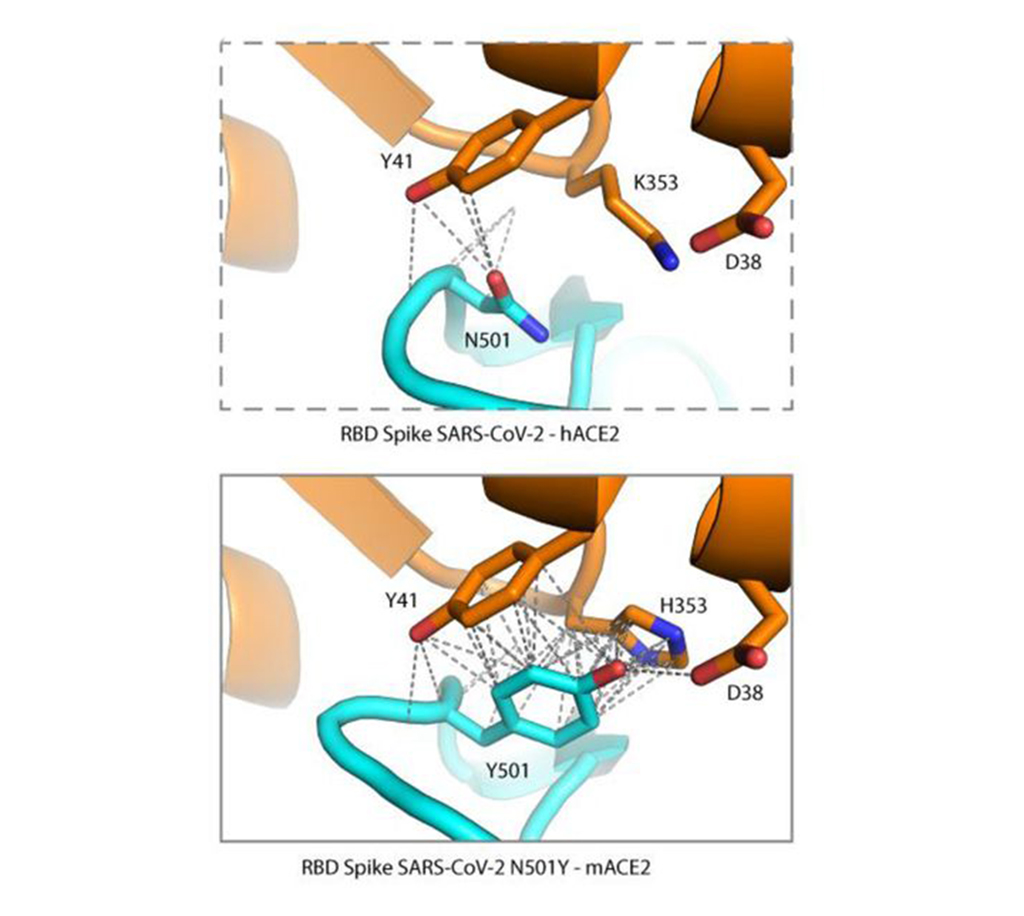
As variantes brasileira e sul-africana conseguem infectar ratos especificamente graças à mutação N501Y (troca de asparagina por tirosina na posição 501 da proteína spike), que melhora a conexão do vírus com os receptores ACE2 murinos. Veja no modelo abaixo:
Apesar da carga viral alta, os ratos infectados desenvolveram Covid assintomática, sem alterações respiratórias. Mas os cientistas ressaltam que as cobaias utilizadas eram bem jovens, com apenas dois meses (a expectativa de vida das linhagens murinas BALB/c e C57BL/6, usadas na experiência, é de 22 a 29 meses). “Ainda é preciso determinar se uma condição mais severa poderia ocorrer em ratos mais velhos”, afirma o estudo. O Sars-CoV-2 é capaz de infectar gatos, furões, visons e civetas – mas, antes da mutação, não afetava ratos.
Não é a primeira vez que mutações em um coronavírus o tornam capaz de infectar novas espécies. Foi assim, afinal, que o Mers-CoV e o primeiro Sars-CoV chegaram ao homem. Mas é a primeira vez que um vírus pandêmico, que está se espalhando em grande escala pela população humana, consegue aperfeiçoar geneticamente sua “zoonose reversa” – e atingir uma espécie previamente imune.


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Por que existe a letra “h” se ela não tem som?
Por que existe a letra “h” se ela não tem som? A cidade subterrânea de 2 mil anos e 8 andares em Derinkuyu, na Turquia
A cidade subterrânea de 2 mil anos e 8 andares em Derinkuyu, na Turquia 9 filmes imperdíveis para assistir no Prime Video
9 filmes imperdíveis para assistir no Prime Video Filtro de luz azul para telas não tem eficácia comprovada
Filtro de luz azul para telas não tem eficácia comprovada Bactérias “vampiras” letais são atraídas por proteína do sangue humano
Bactérias “vampiras” letais são atraídas por proteína do sangue humano