Rússia espera aprovação da Anvisa para vacina contra covid-19 em dezembro
O presidente do Fundo de Investimento Russo, Kirill Dmitriev, participou de uma coletiva de imprensa sobre a produção e distribuição da vacina na América Latina. Saiba as novidades.
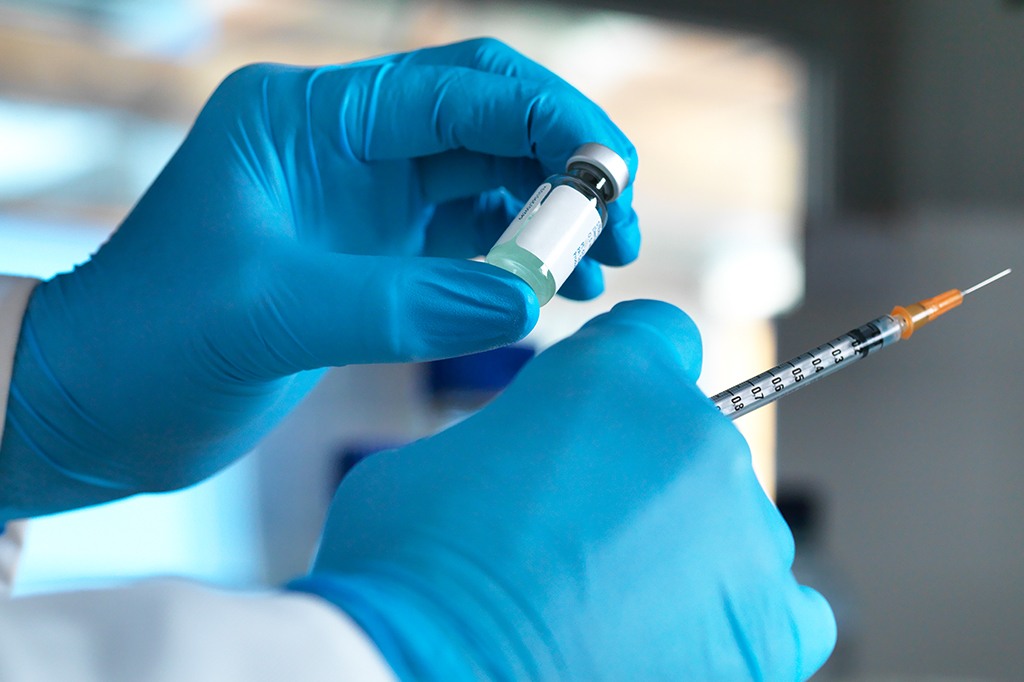
Em agosto, a vacina russa Sputnik V se tornou a primeira aprovada contra a covid-19 – ao menos em seu país de origem. A agência reguladora russa equivalente à Anvisa autorizou sua aplicação em larga escala. Concorrentes como a vacina da Universidade de Oxford e a chinesa Coronavac ainda estão passando pelos testes clínicos, e só foram aplicadas em voluntários.
Apesar da aprovação adiantada, o Instituto Nacional de Pesquisas Gamaleya, que desenvolveu a Sputnik V, ainda está realizando os testes clínicos. 16 mil voluntários russos já participam da terceira fase de estudos, cujo objetivo é verificar a eficácia e segurança da vacina em um grande grupo de pessoas. Quase 40 mil voluntários de diferentes países ainda deverão tomar parte nesta etapa.
O presidente do Fundo de Investimento Russo, Kirill Dmitriev, participou hoje (19) de uma coletiva de imprensa sobre a produção e distribuição da vacina na América Latina. Ele afirmou que os dados dos testes clínicos serão publicados e enviados para a Agência Nacional de Vigilância Sanitária (Anvisa) até dezembro, e que espera receber a aprovação para produzir a vacina no Brasil ainda este ano.
O objetivo do Instituto Gamaleya não é exportar apenas a vacina em si, mas também a tecnologia para a produção do imunizante em outros países. Dmitriev afirmou que a tecnologia já começou a ser transferida para o Brasil, por meio de uma parceria com a farmacêutica União Química, sediada em São Paulo.
“Acreditamos que em dezembro já começaremos a produção. Normalmente, [o início da produção] demoraria de quatro a seis meses, mas tentaremos o menor prazo possível considerando a pandemia”, disse Kirill Dmitriev.
Bahia e Paraná também já fecharam parcerias para que os profissionais de saúde desses estados participem dos testes da Sputnik V, integrando os 40 mil voluntários mencionados antes. No entanto, a Anvisa ainda não aprovou o início dos testes.
Apesar de já ter sido aprovada na Rússia, o país ainda não iniciou a vacinação em massa da população. Quando questionado sobre quantos russos já receberam a vacina fora dos testes clínicos, Dmitriev não deu números, mas afirmou que médicos e grupos de risco estão recebendo a vacina aos poucos. Ele também citou que seus pais, ambos com mais de 70 anos, já receberam a dose.
É importante dizer que, apesar de a vacina já estar sendo aplicada pontualmente em idosos, os testes clínicos ainda não foram realizados com pessoas dessa faixa etária. Os voluntários que participam dos testes até agora possuíam entre 18 e 60 anos. Denis Logunov, diretor adjunto do Instituto Gamaleya, afirmou que o laboratório já recebeu o aval para iniciar os estudos em pessoas com mais de 60 anos, e que esses testes devem começar em breve.
Logunov também ressaltou que nenhum dos voluntários apresentou efeitos colaterais graves até o momento. Os sintomas adversos relatados por algumas pessoas já eram esperados, como hipotermia, dor no local de aplicação e fadiga.
Os resultados das fases 1 e 2 de testes foram publicados em setembro no periódico The Lancet. A primeira fase avalia a segurança da vacina e seus efeitos colaterais em um grupo com algumas dezenas de pessoas. A segunda fase verifica se ela induz a resposta imunológica, com produção de anticorpos, em algumas centenas de voluntários. A terceira fase, em que a Sputnik V se encontra, avalia se o imunizante de fato protege pessoas expostas ao coronavírus.


 Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência
Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência O que está incluso na assinatura do ChatGPT Pro, que custa R$1.200 por mês
O que está incluso na assinatura do ChatGPT Pro, que custa R$1.200 por mês Auto da Compadecida 2: o que você precisa saber antes de assistir ao filme
Auto da Compadecida 2: o que você precisa saber antes de assistir ao filme Estes são os 100 nomes de bebês mais populares de 2017
Estes são os 100 nomes de bebês mais populares de 2017 7 jogos de tabuleiro para dar de presente neste Natal
7 jogos de tabuleiro para dar de presente neste Natal







![[BF2024-PRORROGAMOS] - Paywall - DESKTOP - 728x90](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-DESKTOP-728x90-1.gif)
![[BF2024-PRORROGAMOS] - Paywall - MOBILE - 328x79](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-MOBILE-328x79-1.gif)