Vacinação nacional começa nesta segunda
A Anvisa frisou que não há dados para avaliar se a Coronavac gera imunidade em longo prazo; mas decidiu que os benefícios superam as deficiências.
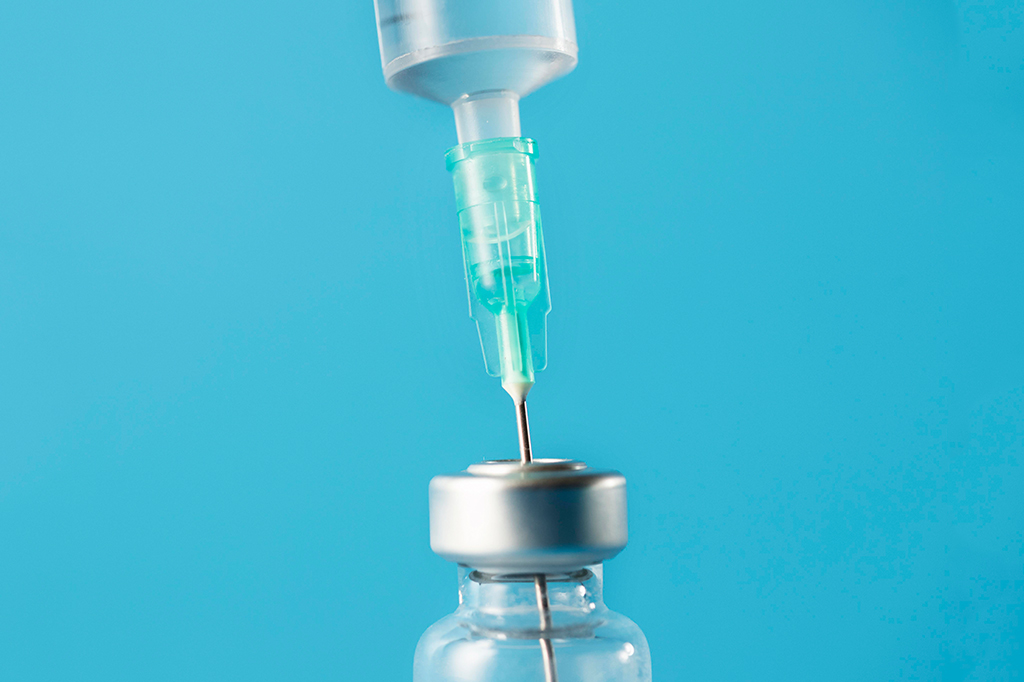
Ao longo desta segunda feira (18), aviões da FAB e voos de companhias aéreas passaram a distribuir 4,5 milhões de doses da Coronavac – partindo do aeroporto de Guarulhos rumo aos outros Estados. O Ministério da Saúde autorizou os governadores que quiserem iniciar seus programas ainda hoje a fazê-lo – originalmente, as primeiras injeções seriam aplicadas só na quarta-feira (20).
No domingo (17) a Anvisa concedeu a autorização de uso emergencial para duas vacinas contra o Sars-CoV-2: a Coronavac, produzida pela empresa chinesa Sinovac em parceria com o Instituto Butantan, e a vacina britânica desenvolvida pela AstraZeneca com a Universidade de Oxford, que será fabricada no Brasil pela Fundação Oswaldo Cruz (Fiocruz).
Os cinco membros da Diretoria Colegiada analisaram os dados de relatórios produzidos pela equipe técnica da Anvisa sobre os dois imunizantes. O pedidos para uso emergencial das duas vacinas foram apresentados no dia 8 de janeiro, e a agência tinha um prazo de dez dias para dar a resposta final a ambos.
Ocorreu uma votação porque o pedido é de uso emergencial, e não definitivo. Em condições normais – leia-se: quando não há uma pandemia ocorrendo –, a área técnica tem autonomia para decidir sozinha se um medicamento ou vacina serão aprovados. Na transmissão de hoje, os especialistas apresentaram dados e argumentos recomendando a aprovação dos dois imunizantes – e os diretores, então, optaram por aprová-los.
O governador de São Paulo, João Dória, acompanhou a reunião no Hospital das Clínicas da Faculdade de Medicina da USP, na capital paulista. Doria iniciou simbolicamente a vacinação no Estado logo após a aprovação da Anvisa. A primeira vacinada foi Mônica Calazans, uma enfermeira de 54 anos com comorbidades que trabalha na UTI do Instituto de Infectologia Emílio Ribas. Nesta segunda, outros profissionais de saúde começaram a receber suas doses.
A primeira vacinada será Mônica Calazans, uma enfermeira de 54 anos com comorbidades que trabalha na UTI do Instituto de Infectologia Emílio Ribas.
É importante frisar que a avaliação das vacinas não acabou. Tanto a Coronavac quanto a vacina de Oxford passaram pelo crivo sob a condição de que, em longo prazo, se faça um monitoramento cuidadoso dos vacinados. Haverá reavaliações periódicas da segurança e da eficácia do imunizante, ainda que, por ora, a agência não veja risco em iniciar sua aplicação em larga escala.
A principal ressalva apresentada pela Anvisa foi a de que o Instituto Butantan não apresentou dados quantitativos satisfatórios sobre a imunogenicidade da Coronavac ao longo do tempo.
Imunogenicidade é um termo utilizado para se referir à capacidade da vacina de gerar uma resposta do sistema imunológico (por meio da produção de anticorpos e a posterior produção de células T de memória, que geram imunidade em longo prazo).
Ou seja: não se sabe por quantos meses a vacina de fato protege. Porém, dada a falta de alternativas mais certeiras, a agência optou pela aprovação.
Outra ressalva à Coronavac foi sua eficácia em idosos. Foram apenas cinco testados: três receberam placebo; dois, a vacina. O número não é suficiente para chegar a conclusões confiáveis. Mas, como o índice geral de eficácia (50.38%) é alto o bastante, isso não atrapalhou a aprovação.
A Anvisa determinou ainda que as doses da vacina de Oxford fabricadas na Índia são, de fato, similares às provenientes do Reino Unido – mas não idênticas, pois a matéria-prima (os adenovírus usados para carregar a proteína que gera a resposta imunológica) vêm de um banco de vírus diferente. A Fiocruz importará 2 milhões de doses da versão indiana, fabricada no Insituto Serum, e também produzirá doses em território nacional.
A agência foi transparente ao apresentar as limitações encontradas nos testes clínicos. No caso da Coronavac, cerca de 2 mil voluntários não voltaram para receber a segunda dose.
Já no caso da vacina de Oxford, houve um problema na determinação das doses ministradas aos voluntários. Algumas pessoas receberam as duas doses, outras receberam o equivalente a uma dose e meia. A dose menor gerou uma resposta imune melhor, algo peculiar que será considerado em avaliações futuras.
Ao longo dos últimos dias, a Anvisa vinha analisando os documentos enviados tanto pela Fiocruz como pelo Butantan e atualizando em tempo real o status da empreitada. Em alguns pontos, a área técnica da Anvisa pedia esclarecimentos ou dados adicionais aos institutos de pesquisa durante a análise. Na sexta-feira (15), por exemplo, só 45% da análise da documentação da Coronavac havia sido concluída; outros 44% estavam sob análise e cerca de 11% dos papeis estavam com a tramitação parada por falta de dados.
As estão liberadas. A aprovação para uso emergencial, porém, só permite que as vacinas sejam disponibilizadas no sistema público de saúde. A comercialização é proibida. O sistema privado, por enquanto, fica de fora.
O governo federal, que vinha apostando suas fichas na vacina de Oxford, afirmou que a campanha de vacinação nacional poderia começar, na melhor das hipóteses, no dia 20. No entanto, ainda não foram divulgados detalhes do plano. O ministro da Saúde, Eduardo Pazuello, foi bastante criticado por não anunciar um calendário concreto na semana passada – falou apenas que a vacinação começaria “no dia D e na hora H”.
O governo de São Paulo já tem em mãos aproximadamentes 6 milhões de doses da Coronavac. 4,5 milhões deverão ser distribuídas para o resto do País. Além das doses compradas no exterior, o Brasil passará a produzir suas próprias vacinas. Até o fim de 2021, o governo federal espera contar com mais de 200 milhões de doses da vacina da Fiocruz, e já negociou quase 100 milhões de doses da Coronavac com o Butantan.
Na semana passada, o Butatan anunciou que a eficácia geral da Coronavac é de 50,38% – pouco acima dos 50% exigidos pela Anvisa para aprovação, valor que também é recomendado pela Organização Mundial da Saúde (OMS).
Apesar de o número ser considerado bom para frear a pandemia e, principalmente, suficiente para evitar uma explosão de casos graves e moderados, a taxa foi menor que o esperado para muitos, especialmente após o Butatan divulgar a taxa parcial de 78% de proteção (que se refere apenas a casos com sintomas relevantes) antes do anúncio oficial.
A vacina Oxford/AstraZeneca também passou por uma polêmica em relação a sua eficácia. Atualmente, o valor está definido 70,4%. O problema é que, nos testes clínicos, percebeu-se que a eficácia variava em subgrupos que tomaram doses diferentes em intervalos de tempo diferentes.
O resultado foi de 62% até um máximo de 90%, embora esse segundo número só tenha sido atingido em um subgrupo muito menor de pessoas – e, por isso, não tenha tanta relevância estatística. Devido a essas diferenças nos regimes de dosagem durante os estudos, que aconteceram por falhas de planejamento, não se sabe exatamente qual é a eficácia da vacina.
Até o momento, a Indonésia e a Turquia já concederam aprovação de uso emergencial para a Coronavac e começaram sua aplicação em suas populações. Já a vacina de Oxford foi aprovada primeiro no Reino Unido, onde já está sendo usada, e também recebeu aval na Índia, Argentina e México.
Texto atualizado na segunda (18), 15h10


 “Cem Anos de Solidão”: entenda a árvore genealógica da família Buendía
“Cem Anos de Solidão”: entenda a árvore genealógica da família Buendía Estes são os 100 nomes de bebês mais populares de 2017
Estes são os 100 nomes de bebês mais populares de 2017 7 jogos de tabuleiro para dar de presente neste Natal
7 jogos de tabuleiro para dar de presente neste Natal Conheça a única raça brasileira de gato – confundida com “vira-lata”
Conheça a única raça brasileira de gato – confundida com “vira-lata” Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência
Os gatos fazem bem para a nossa saúde? Veja o que diz a ciência







![[BF2024-PRORROGAMOS] - Paywall - DESKTOP - 728x90](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-DESKTOP-728x90-1.gif)
![[BF2024-PRORROGAMOS] - Paywall - MOBILE - 328x79](https://super.abril.com.br/wp-content/uploads/2024/12/BF2024-PRORROGAMOS-Paywall-MOBILE-328x79-1.gif)