Ordem da FDA gera impasse envolvendo as novas vacinas contra a Ômicron
A Pfizer e a Moderna apresentaram vacinas atualizadas, mas nem tanto: são baseadas na Ômicron BA.1, que já foi extinta. A FDA quer imunizantes contra as subvariantes BA.4 e BA.5, as mais comuns hoje. Está certíssima. Mas isso também cria um dilema. Entenda por que.
A Pfizer e a Moderna apresentaram vacinas atualizadas, mas nem tanto: são baseadas na Ômicron BA.1, que já foi extinta. A FDA não engoliu: ela quer imunizantes contra as subvariantes BA.4 e BA.5, as mais comuns hoje. Está certíssima. Mas isso também cria um dilema. Entenda por que.
Você deve se lembrar. No começo de junho, o laboratório americano Moderna finalmente anunciou a primeira vacina atualizada contra a variante Ômicron. A novidade foi recebida com otimismo, e depois com certa decepção: o imunizante era baseado na Ômicron BA.1, que já foi extinta. Alguns dias mais tarde, a Moderna disse que sua nova vacina também funciona contra as subvariantes BA.4 e BA.5, mais recentes e comuns, mas com menos potência: gera um nível de anticorpos 3 vezes menor.
Depois foi a vez da Pfizer, que anunciou a mesma coisa. Ela também baseou sua nova vacina na Ômicron BA.1. O imunizante também age contra BA.4 e BA.5, mas também perde potência: produz 3 vezes menos anticorpos neutralizantes contra essas subvariantes (comparando com o efeito anti-BA.1).
Acontece que as variantes BA.4 e BA.5 devem se tornar dominantes, no mundo todo, nos próximos meses. No Brasil, elas já são. Um levantamento do Instituto Todos pela Saúde (ITpS), que analisou mais de 150 mil testes de Covid realizados em vários estados do país durante os últimos meses, revelou que essas subvariantes estavam presentes em 93,2% das amostras na primeira semana de julho.
Em suma: a BA.4 e a BA.5 são a nova realidade da pandemia. E a nova geração de vacinas já nasceu bem defasada contra elas.
Isso é um problema. As subvariantes pós-BA.1 carregam mutações importantes, que parecem dar a elas um alto grau de “escape imunológico” – a capacidade de driblar os anticorpos induzidos pelas vacinas atuais (ou pela infecção por variantes mais antigas do Sars-CoV-2). Se a humanidade for produzir e tomar vacinas atualizadas, é vital que elas sejam baseadas nas Ômicrons mais recentes.
A FDA também pensa assim, e resolveu colocar ordem na casa: disse que as empresas farmacêuticas que “estão querendo atualizar suas vacinas contra a Covid-19” devem trabalhar mais um pouco, e desenvolver imunizantes contendo “um componente da [proteína] spike omicron BA.4/5″. Pfizer e Moderna terão de reescrever o código mRNA das suas novas vacinas, para que elas ensinem o organismo a produzir a spike da Ômicron BA.4 e BA.5 – e não apenas da BA.1.
O comunicado da FDA é um pouco ambíguo, e não diz categoricamente que a agência irá vetar as vacinas BA.1, que já foram desenvolvidas e testadas. Ela dá a entender que pode vetar, mas não crava. E isso cria um impasse. Quando teremos vacinas atualizadas para a Ômicron? E, mais importante, baseadas em quais subvariantes? A velha e extinta, ou as novas e dominantes?
Os laboratórios querem lançar novos imunizantes em tempo para o inverno americano, mas o tempo está correndo – e as decisões tomadas pela FDA e por eles nas próximas semanas irão determinar se a nova vacina já nascerá antiga (BA.1), ou será mais atual (BA.4/5).

Procurada pela Super, a Pfizer afirmou que sua “plataforma mRNA permite atualizar rapidamente a vacina”, e disse que terá um novo imunizante contra BA.4 e BA.5. “Estamos prontos para distribuir a vacina ao mundo até início de outubro de 2022, dependendo das autorizações regulatórias.” Só que existe um detalhe crítico envolvendo esse prazo de outubro, que você vai entender agora.
A Moderna afirmou que já está desenvolvendo uma vacina atualizada. “As entregas da vacina bivalente BA.4/BA.5 podem começar em outubro, assumindo um processo de aprovação acelerado, sem dados clínicos”, disse a empresa em nota à Super. Sem dados clínicos, eis aí o ponto-chave.
A Moderna está dizendo que ela pode começar a fornecer a vacina BA.4/5 em outubro, em tempo para o inverno americano – mas não daria tempo de fazer um teste clínico completo, em que centenas ou milhares de voluntários são acompanhados durante alguns meses. A FDA teria que aprovar a vacina com base em dados pré-clínicos (como ensaios de laboratório e testes em animais).
Perguntada a respeito, a Pfizer não respondeu. Mas é extremamente provável que sua situação seja a mesma, por uma razão simples: fazer testes clínicos leva tempo. Você precisa monitorar as pessoas durante um certo período, no qual elas levam suas vidas e acabam se expondo ao Sars-CoV-2, para saber se a vacina de fato reduziu a taxa de infecções e hospitalizações (mais do que o placebo). Não há como acelerar esse processo.
Então chegamos a uma encruzilhada. Se a FDA autoriza as vacinas BA.1, elas já nascem bem atrás da Ômicron. Podem até ser melhores do que as vacinas atuais, ok – mas, com sua defasagem inicial considerável e o ritmo de evolução do Sars-CoV-2, por quanto tempo se manterão eficazes?
Vale lembrar que as vacinas atuais (baseadas no coronavírus original, o de Wuhan) continuam oferecendo boa proteção contra doença severa. Na prática, vacinas BA.1 proporcionariam uma vantagem real?
Já se a FDA faz o contrário, e bate o pé para exigir vacinas atualizadas contra BA.4/5, aí o problema é outro: elas terão de ser liberadas sem os testes clínicos, o que não é bom, ou então demorarão vários meses a mais – quando chegarem, talvez já existam variantes pós-BA.4/5, que poderão reduzir (no pior cenário, comprometer) a eficácia dessas novas vacinas.
Isso mostra que a estratégia atual, de tentar desenvolver vacinas adaptadas a novas variantes, talvez não seja sustentável a longo prazo – porque mesmo com a agilidade da tecnologia mRNA, o processo demora um pouco. E isso acaba criando janelas de tempo em que o vírus pode incorporar mutações e escapar dos novos imunizantes.
Para de fato controlar o Sars-CoV-2, provavelmente vamos precisar de outras armas – como uma vacina “pan-coronavírus”, que dê alguma proteção contra variantes que ainda nem existem. Nesta semana, cientistas do Instituto de Tecnologia da Califórnia (Caltech) conseguiram demonstrar algo parecido com isso.
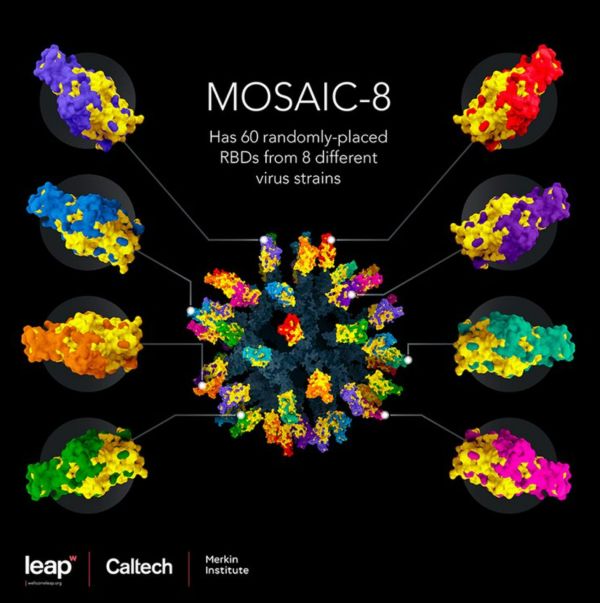
Eles anunciaram que sua vacina experimental, a Mosaic-8, se mostrou eficaz em testes com macacos – eles ficaram protegidos até contra um vírus que não é representado na vacina. Essa vacina (sobre a qual falamos pela primeira vez na reportagem “O futuro da Covid”, em fevereiro) contém pedaços da proteína spike de oito coronavírus: o Sars-CoV-2 (variante Beta) e mais sete, que infectam animais.
As amostras dos oito vírus são “grudadas” em uma nanopartícula: são ao todo 60 pedacinhos, distribuídos como em um mosaico (daí o nome da vacina).
Nos testes em macacos, a Mosaic-8 conseguiu fazer algo surpreendente: gerou proteção até contra outros vírus, que não estavam presentes na vacina – como o Sars-CoV-1 e a variante Ômicron do Sars-CoV-2 (nos subtipos BA.4 e BA.5).
Se essa vacina se mostrar segura e eficaz em humanos, ela poderá transformar completamente o enfrentamento da pandemia. Em vez de ficar correndo atrás do coronavírus, tentando acompanhar o surgimento de novas variantes, a humanidade teria uma arma contra todas as variantes do Sars-CoV-2 – inclusive as que ainda não existem.
Mas os testes da Mosaic-8 ainda vão demorar. Bem mais, com certeza, do que o desenvolvimento das próximas vacinas da Pfizer e da Moderna – seja qual for o caminho adotado por elas e pela FDA.


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Estudo revela que populações indígenas envelhecem com menos inflamação
Estudo revela que populações indígenas envelhecem com menos inflamação Orcas são filmadas oferecendo peixes a humanos. É presente ou manipulação?
Orcas são filmadas oferecendo peixes a humanos. É presente ou manipulação? Como pássaros parasitas, sem pais, descobrem qual é sua espécie?
Como pássaros parasitas, sem pais, descobrem qual é sua espécie? No Brasil, os vira-latas reinam soberanos – e se chamam Mel, Luna e Thor
No Brasil, os vira-latas reinam soberanos – e se chamam Mel, Luna e Thor Cientistas decifram significado de gestos que elefantes fazem com as trombas
Cientistas decifram significado de gestos que elefantes fazem com as trombas







